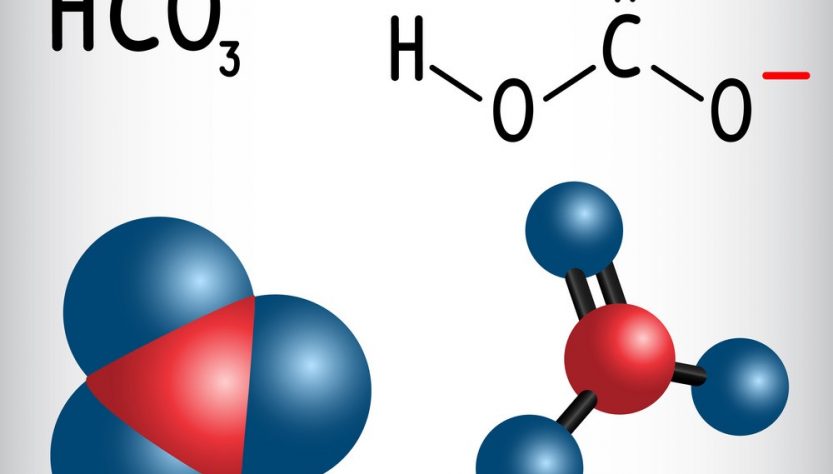
Trong hóa học vô cơ, Bicacbonat, còn gọi là bicarbonate (IUPAC – Danh pháp khuyến nghị: hydro cacbonat ) là một hình thức deprotonation trung gian của axit carbonic. Nó là một anion đa nguyên tử có công thức hóa học là HCO−3, những chất nào phản ứng với nhau để tạo thành HCO3 dưới đây chúng tôi sẽ hướng dẫn các bạn cách viết phương trình hóa học cân bằng CO2 + CO3 + H2O = HCO3 , Mời các bạn cùng theo dõi.
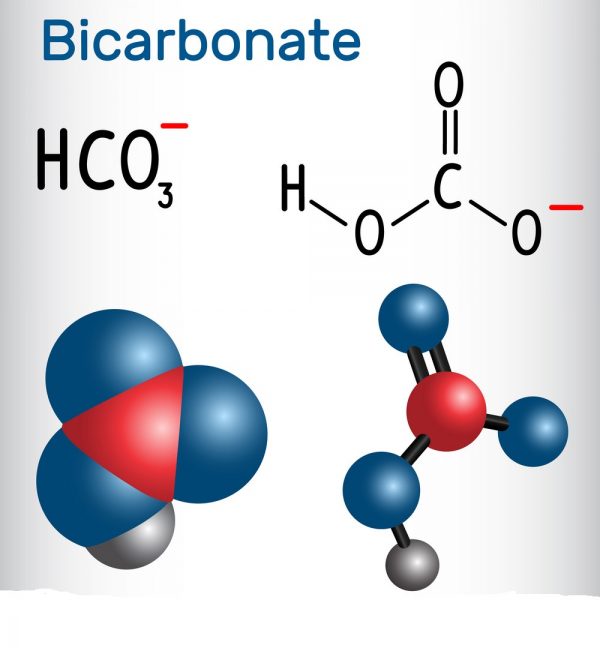
- 2C2H5OH + 2CO2 → C6H12O6
- H2(CO3) → H2O+ CO2 Phản ứng hóa học sau khi Phân hủy
- Canxi ( Ca ) hóa trị mấy?
Bicarbonate đóng một vai trò sinh hóa quan trọng trong hệ thống đệm pH sinh lý. Trên mỗi ion natri trong natri bicacbonat (NaHCO3) và các muối bicacbonat khác với trong natri cacbonat (Na2CO3) và các muối cacbonat khác.
Phương trình phản ứng hóa học :
CO2 + CO3 + H2O = HCO3
Đây là phản ứng tổng hợp của nước tác dụng với cacbon ddioxxxit và carbon trioxide để tạo ra HCO3
Tính chất của HCO3 :
Canxi bicacbonat tồn tại dạng dung dịch màu trong suốt. Để nhận biết hợp chất này, người ta sử dụng dung dịch HCl, chất tạo thành là khí không màu, không mùi.
PTHH: Ca(HCO3)2 + 2HCl CaCl2 + 2H2O + 2CO2
Một số tính chất hóa học của Canxi bicacbonat có thể kể đến như sau:
Tác dụng với axit mạnh: Ca(HCO3)2 + H2SO4 CaSO4 + 2H2O + 2CO2
Tác dụng với bazơ:
Ca(HCO3)2 + Ca(OH)2 2CaCO3 + 2H2O
Ca(HCO3)2 + 2NaOH CaCO3 + Na2CO3 + 2H2O
Nhiệt phân Ca(HCO3)2
Ca(HCO3)2 CaCO3 + H2O + CO2
Nhiều người thường thắc mắc Ca(HCO3)2 có kết tủa không?. Câu trả lời là không. Vì Canxi bicacbonat tan tốt trong nước nên không phải là kết tủa.
Các phương trình phản ứng cân bằng khác :